随着高通量技术的发展,肿瘤发生的分子机制逐渐被揭示。其中肿瘤抑制因子FBW7是能介导致癌基因蛋白降解的SCF E3泛素连接酶复合物的潜在识别成分。然而FBW7在肿瘤中发挥怎样的作用仍未被阐明。2021年3月3日,云序客户复旦大学附属肿瘤医院吴小华教授课题组在Molecular Cancer 上在线发表题为“FBW7 suppresses ovarian cancer development by targeting the N6-methyladenosine binding protein YTHDF2”的研究论文,该研究运用云序生物m6A- meRIP-seq和RNA-seq等方法发现FBW7能够通过YTHDF2介导的BMF mRNA降解抑制卵巢癌肿瘤的生长和发展。该结果具有重要的临床意义,为抗癌疗法的未来发展提供了重要的理论基础。

影响因子:15.302
研究方法:m6A- meRIP-seq、RNA-seq
文章链接:FBW7 suppresses ovarian cancer development by targeting the N 6-methyladenosine binding protein YTHDF2
研究内容
(1)人类卵巢癌中FBW7下调与不良预后和m6A修饰水平下调相关。
作者比较了FBW7在癌变和非癌变卵巢组织中的表达发现FBW7在卵巢癌组织中下调(图1a、b)。通过免疫组化(IHC)染色,分析FBW7在包含120个肿瘤样本的卵巢癌组织芯片中的表达情况,将卵巢癌样本分为两类FBW7低、高表达组(图1c、d)。然后作者探讨了FBW7表达与卵巢癌临床病理特征的关系Kaplan-Meier生存分析显示,高水平的FBW7与良好的卵巢癌总生存期相关(图1e, P = 0.04)。此外,高水平的FBW7与更好的无进展生存(PFS)呈正相关,但不明显(图1f)。因此,这些观察结果表明FBW7是一种可能抑制卵巢肿瘤发生和发展的良好预后标志物。为了研究m6A修饰是否影响FBW7的调控,作者测定了60个人卵巢癌组织样本中的m6A水平。发现在FBW7表达水平较高的肿瘤患者中,m6A水平升高(图1g),且较好的总生存率与较高的m6A水平相关(图1h),表明FBW7可能受m6A调控。
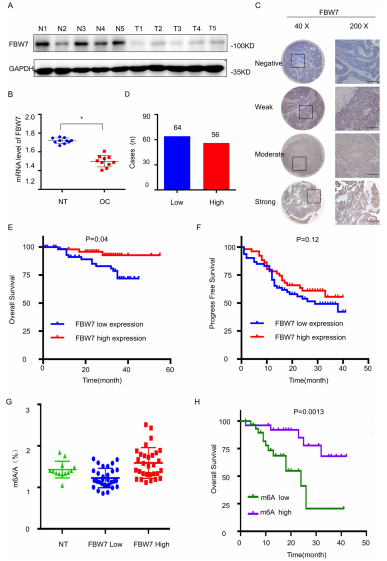
(2)FBW7作为肿瘤抑制因子抑制卵巢癌细胞增殖
为了研究FBW7在卵巢癌中的生物学功能,作者在SKOV3和OVCAR429细胞系中创建了FBW7稳定过表达系维持内源性FBW7低表达水平(图2a)。过表达FBW7抑制卵巢癌细胞增殖(图2b)、集落形成(图2c)和细胞生长(图2d)能力。肿瘤抑制活性可能归因于诱导凋亡,因为异常表达的FBW7增加了Annexin Vpositive细胞数量(图2e)。此外,作者建立了一种异种移植小鼠模型来检测FBW7是否在体内抑制了卵巢肿瘤的生长。结果显示,相比于对照组异位FBW7抑制小鼠肿瘤生长(图2f),其肿瘤体积和重量均有抑制(图2g和h)。此外,敲除FBW7促进卵巢癌细胞增殖、集落形成和细胞生长的能力。这些结果说明FBW7在卵巢癌中具有抑瘤作用。
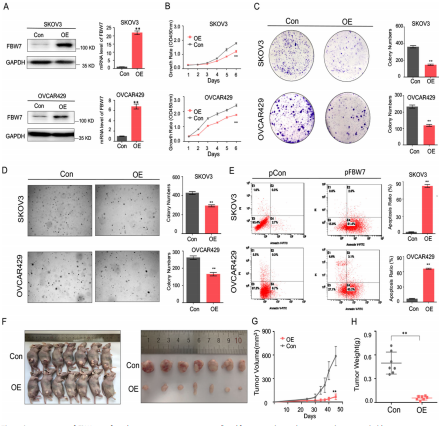
(3)FBW7诱导YTHDF2泛素化和蛋白酶体降解。
为了阐明FBW7介导的m6A修饰系统的分子机制,作者进行了FBW7抗体的Co-IP实验和质谱分析证实了FBW7与SKOV3癌细胞中的YTHDF2结合(图3a)。免疫荧光(IF)染色提示相互作用可能发生在细胞质中(图3b)。FBW7是否通过相互作用调节YTHDF2蛋白的稳定性。过表达FBW7后YTHDF2蛋白水平明显下降,而通过蛋白酶体抑制剂MG132处理细胞后,这种下降完全恢复(图3c)。此外,由环己酰亚胺追逐实验可知FBW7过表达缩短了YTHDF2的半衰期(图3d)。此外也发现FBW7提高了YTHDF2的泛素化(图3e),这在另一组使用抗YTHDF2抗体的泛素化实验中得到证实(图3f)。上述结果说明在卵巢癌中,FBW7促进YTHDF2泛素化介导的蛋白降解来调节m6A修饰系统。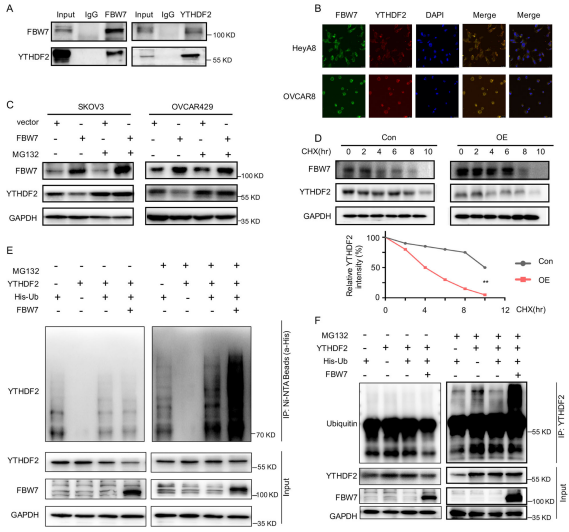
(4)YTHDF2与卵巢癌FBW7表达及预后呈负相关
由于YTHDF2是肿瘤抑制因子FBW7降解的底物,那么是否这两种蛋白之间的负相关也存在于原发性卵巢癌组织中?首先,作者发现YTHDF2在卵巢癌中表达升高(图4a)。此外YTHDF2的表达与FBW7之间存在负相关(图4b和c)。根据YTHDF2的表达水平将肿瘤标本分为两组(图4d),分析各组的临床病理特征。Kaplan-Meier生存分析显示YTHDF2表达增加与卵巢癌较差的总生存期(OS)相关(图4e)。然而,YTHDF2并不是无进展生存期(PFS)的一个合适的预后指标(图4 f)。FBW7高表达/YTHDF2低表达组OS优于FBW7低表达/YTHDF2高表达组。在多变量分析中,YTHDF2的表达是OS的不利的独立预后因子。这些结果标明YTHDF2可能促进卵巢癌的生存和生长。
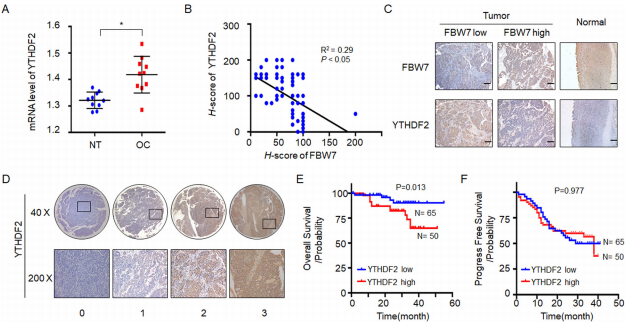
(5)YTHDF2在卵巢癌中是一种致癌蛋白
为了验证这个YTHDF2参与卵巢癌的发展,作者在SKOV3和OVCAR420细胞系中创制了两种独立的ythdf2缺失株系(图5a)。结果发现ythdf2缺失抑制了细胞增殖(图5b)、集落形成(图5b)和细胞生长能力(图5d)。此外,流式细胞仪分析显示,ythdf2缺失可诱导卵巢癌细胞凋亡(图5e)。此外,异种移植小鼠模型显示ythdf2缺失抑制了体内卵巢肿瘤的生长(图5f),导致肿瘤体积和重量减少(图5g和h)。并且敲除YTHDF2恢复了由FBW7降解诱导的细胞增殖和集落形成能力(图5i-k)。上述结果说明YTHDF2可能驱动卵巢癌的发展,而FBW7通过诱导蛋白降解抑制卵巢癌的发生,从而降低其致癌活性。
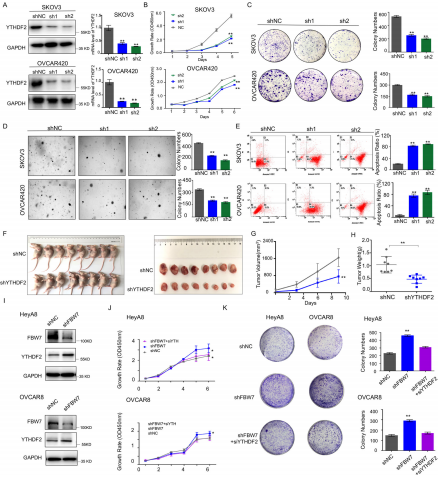
(6)BMF是FBW7-YTHDF2的级联效应因子
YTHDF2被证明会促使m6A修饰转录本的衰变,那么FBW7是否通过抑制YTHDF2调节细胞m6A富集?采用LC-MS/MS法定量m6A水平,发现YTHDF2的敲除增加了卵巢癌细胞系(图6a)中m6A丰度。FBW7过表达导致m6A升高(图6b)。作者还确定了FBW7介导调控m6A丰度依赖于YTHDF2,YTHDF2的敲除中和了FBW7敲除对m6A水平的影响(图6c)。通过RNA-seq发现敲除YTHDF2导致SKOV3细胞中348个基因表达上调,320个基因表达下调(图6d)。m6A- meRIP-seq检测了ythdf2敲除细胞系和正常细胞系结果表明,m6A峰主要位于CDS区(42.3%)(图6 e)。m6A motif序列为GGAC [U/A](图6f),表明YTHDF2也可能在卵巢癌中与m6A结合。通过结合RNA-seq和m6A- meRIP-seq结果发现YTHDF2敲除后有25个基因中有39个峰持续升高(图6g)。在这些异常调节的基因中,BMF是编码一个促凋亡的BH3-only Bcl2家族蛋白,与对照组相比,BMF在YTHDF2敲除后表现出更高的峰富集(图6 h)。进一步证实YTHDF2的敲除提高了BMF mRNA的表达水平并延长了其半衰期(图6j),说明BMF mRNA是YTHDF2降解的靶点。由于m6A修饰是YTHDF2诱导的mRNA衰减必不可少的,那么是否m6A降低BMF mRNA的稳定性?如图6k所示,用甲基化抑制剂处理SKOV3细胞后,BMF mRNA水平升高,表明甲基化对BMF mRNA的降解至关重要(图6k)。
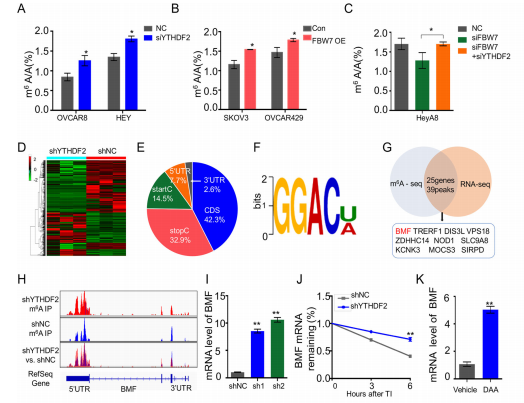
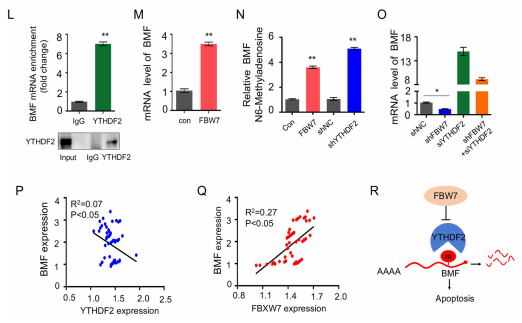
RIP检测证明了YTHDF2与BMF的互作(图6l)。YTHDF2过表达降低了BMF的表达。YTHDF2对细胞增殖和凋亡的影响可以通过恢复BMF表达来逆转。此外,FBW7的过表达与YTHDF2的下调一样,诱导了BMF mRNA水平(图6m),这是由于FBW7降解YTHDF2(图3c-f)。此外,FBW7的过表达或敲除YTHDF2增加了m6A修饰的水平(图6n)。FBW7介导的BMF调控依赖于YTHDF2(图6o)。与这些体外结果一致,作者也揭示了在卵巢癌组织中BMF的表达与YTHDF2表达呈负相关(图6p),而与FBW7表达呈正相关(图6q)。上述结果表明,FBW7通过在卵巢癌中的阅读蛋白YTHDF2调节m6A的一种依赖机制刺激促凋亡BMF的表达(图6r)。
总结
这篇文章结合 LC-MS/MS、m6A-meRIP-seq、RNA-seq、RIP等实验手段探究了FBW7通过调节在卵巢癌中的阅读蛋白YTHDF2来调控m6A修饰水平进而刺激促凋亡基因BMF的表达。该研究表明YTHDF2是潜在的癌症治疗靶标,为靶向治疗癌症提供了新的思路。
云序生物m6A修饰研究五大模块
01 m6A RNA修饰测序
m6A RNA修饰测序(m6A-meRIP-seq)
对m6A RNA甲基化,目前流行的检测手段为m6A-Seq技术,适用于m6A RNA甲基化谱研究,快速筛选m6A RNA甲基化靶基因。云序可提供mRNA和多种非编码RNA的m6A测序:
- m6A 全转录组测序(涵盖mRNA,LncRNA,circRNA)
- m6A LncRNA测序(涵盖LncRNA和mRNA)
- m6A Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
- m6A mRNA测序
- m6A miRNA测序
LC-MS/MS检测整体RNA修饰水平
精准高效,可以实现一次检测,9类修饰水平检测,一步到位。
比色法
快速检测m6A整体甲基化水平
03 m6A RNA修饰上游酶的筛选
m6A RNA修饰相关酶PCR芯片
寻找上游直接调控m6A RNA甲基化的甲基转移酶。
04 m6A RNA修饰靶基因验证
05机制互作研究
5.1 RIP-seq/qPCR
筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
5.2 RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
5.3 双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。
5.4 ChIP-seq
筛选或验证目标蛋白与DNA互作,研究相应的分子调控机制。
云序生物服务优势
优势一:发表10分以上文章多的m6A RNA甲基化测序服务平台。云序已累计支持客户发表42篇高水平文章,合计影响因子300分+,是国内支持发文多、累计影响因子高的公司。
优势二:至今完成4000+例 m6A测序样本,覆盖医口、农口等各类样本。
优势三:检测mRNA和各类非编码RNA(circRNA,lncRNA,Pri-miRNA等)。
优势四:提供m6A一站式服务:m6A整体水平检测、m6A测序、MeRIP-qPCR验证、RIP和RNA pull-down。
优势五:率先研发超微量meRIP测序技术,RNA量低至500ng起。
优势六:国内RNA修饰测序平台,提供m6A、m5C、m1A、m7G、m3C、O8G、ac4C乙酰化和2'-O-甲基化测序。
云序客户RNA修饰文章列表
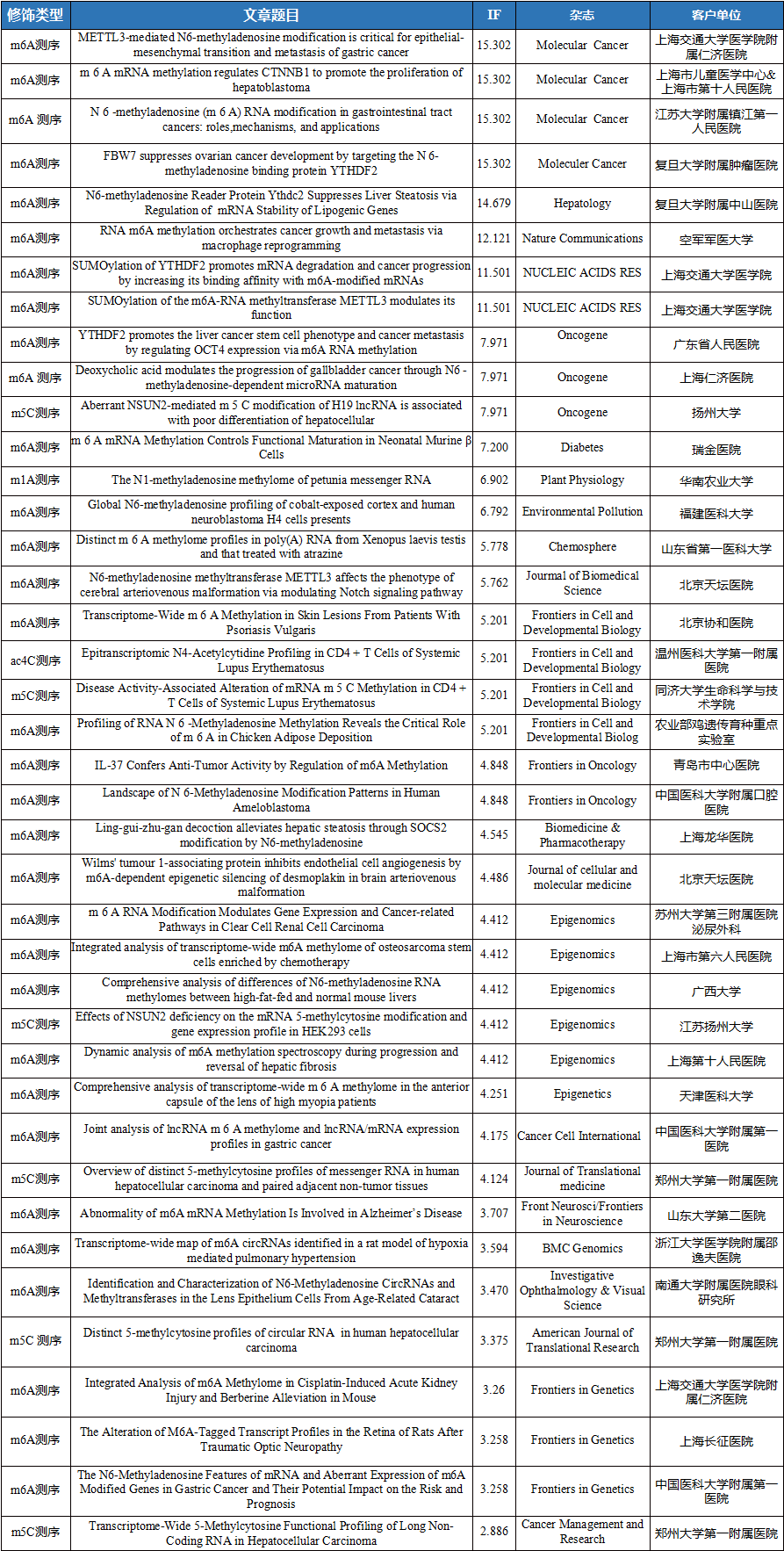
相关产品
往期回顾
Science新发现 |RNA以m6A依赖方式调节染色质状态和基因转录
上海云序生物科技有限公司 商家主页
地 址: 上海市松江区莘砖公路518号24号楼4楼
联系人: 戴小姐
电 话: 021-64878766
传 真: 021-64878766
Email:market@cloud-seq.com.cn;liuqingqing@cloud-seq.com.cn
